教育
Education
研究活動
研究内容
代表的な論文の内容を以下に解説します。
Watanabe M, Sinha AS, Shinmyo Y*, Fukuda A*. Early establishment of chloride homeostasis in CRH neurons is altered by prenatal stress leading to fetal HPA dysregulation. Frontiers in Molecular Neuroscience, 2024, 17: 1373337.
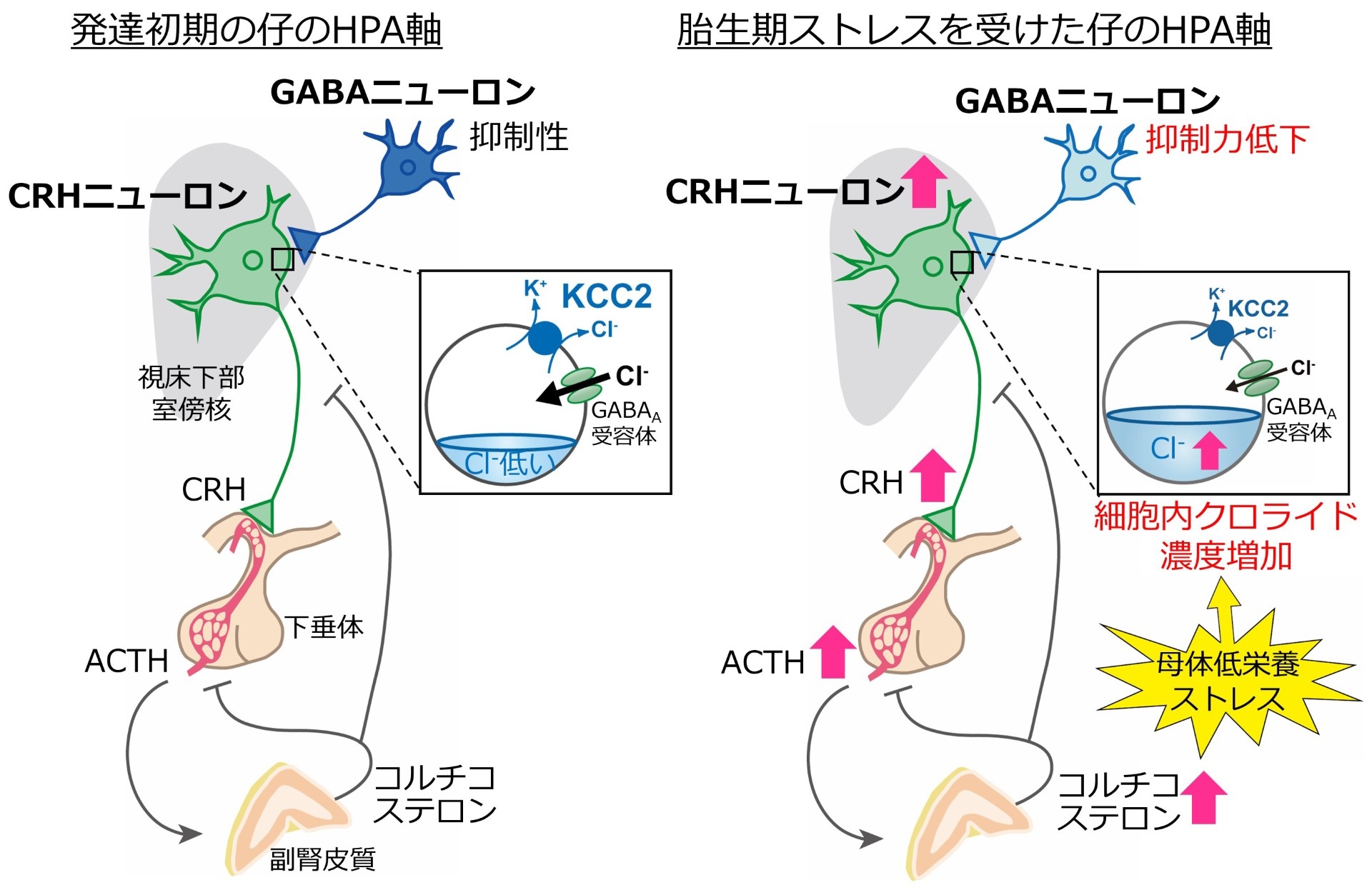 視床下部室傍核にある副腎皮質刺激ホルモン放出ホルモン (CRH) ニューロンは、ストレス応答の中心的な役割を担っている。ストレスを受けるとCRH ニューロンの活動が高まりCRHが分泌され、その結果、下垂体から副腎皮質刺激ホルモン(ACTH)が分泌され、副腎皮質からのコルチコステロン分泌が増加し、生体防御反応が起こる(視床下部-下垂体-副腎軸(HPA軸); 図)。成体マウスではCRHニューロンの活動はγアミノ酪酸(GABA)の働きにより制御されているが、本研究ではGABAによる制御が脳の発達過程のどの時期に完成するか調べた。多くの神経細胞では発達期にはGABAは興奮性に働いているが、生後1-2週の間にCl-を細胞外にくみ出すカリウム−クロライド共輸送体(KCC2)が発現することにより、細胞内クロライド濃度が低くなり、GABA作用は抑制性に変化する。しかし、CRHニューロンでは胎生期にKCC2がすでに発現しているため、GABAは抑制性に作用しており、生後1週で、さらに抑制力が強くなることがわかった。妊娠中のストレスが子供のHPA軸に影響し、将来の精神疾患発症のリスクを高めることが示唆されているが、母体に低栄養ストレスを負荷したところ、仔のHPA軸の亢進がみられ、その要因はCRHニューロンの細胞内クロライド濃度が高くなることによるGABAの抑制力の低下であることがわかった。よって、他の脳部位と比べて、CRHニューロンの細胞内クロライド維持機構は早期に完成し、母体ストレスによりクロライド維持機構が破綻し、HPA 軸の亢進が起こることが明らかになった。
視床下部室傍核にある副腎皮質刺激ホルモン放出ホルモン (CRH) ニューロンは、ストレス応答の中心的な役割を担っている。ストレスを受けるとCRH ニューロンの活動が高まりCRHが分泌され、その結果、下垂体から副腎皮質刺激ホルモン(ACTH)が分泌され、副腎皮質からのコルチコステロン分泌が増加し、生体防御反応が起こる(視床下部-下垂体-副腎軸(HPA軸); 図)。成体マウスではCRHニューロンの活動はγアミノ酪酸(GABA)の働きにより制御されているが、本研究ではGABAによる制御が脳の発達過程のどの時期に完成するか調べた。多くの神経細胞では発達期にはGABAは興奮性に働いているが、生後1-2週の間にCl-を細胞外にくみ出すカリウム−クロライド共輸送体(KCC2)が発現することにより、細胞内クロライド濃度が低くなり、GABA作用は抑制性に変化する。しかし、CRHニューロンでは胎生期にKCC2がすでに発現しているため、GABAは抑制性に作用しており、生後1週で、さらに抑制力が強くなることがわかった。妊娠中のストレスが子供のHPA軸に影響し、将来の精神疾患発症のリスクを高めることが示唆されているが、母体に低栄養ストレスを負荷したところ、仔のHPA軸の亢進がみられ、その要因はCRHニューロンの細胞内クロライド濃度が高くなることによるGABAの抑制力の低下であることがわかった。よって、他の脳部位と比べて、CRHニューロンの細胞内クロライド維持機構は早期に完成し、母体ストレスによりクロライド維持機構が破綻し、HPA 軸の亢進が起こることが明らかになった。
*Shinmyo Y. (Co-corresponding author), Saito K., Hamabe-Horiike T., Kameya N., Ando A., Kawasaki K., Dinh Duong T.A., Sakashita M., Roboon J., Hattori T., Kannon T., Hosomichi K., Slezak M., Holt M.G., Tajima A., Hori O. and Kawasaki H. Localized astrogenesis regulates gyrification of the cerebral cortex. Science Advances, 2022, 8(10):eabi5209.
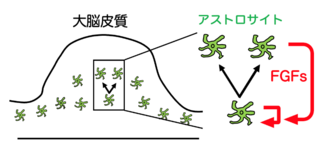
哺乳動物の進化の過程で大脳は肥大化し、脳回脳溝を獲得するなどその構造は複雑化してきた。この進化の過程で、神経細胞に加えてグリア細胞の数は著しく増加するとともに、その形態と機能も発達してきた。従って、進化におけるグリア細胞の変化がヒトの脳に見られる複雑化した脳構造と高次脳機能の獲得に重要であったと考えられるため、皺脳動物(脳回脳溝などの発達した脳構造を持つ動物)でのグリア細胞の研究は重要である。本論文では、FGFシグナルのポジティブフィードバックループによるアストロサイトの増殖制御が進化におけるアストロサイト数の増加に重要であったことを明らかにした(図)。さらに、大脳白質における局所的なアストロサイトの産生が脳回脳溝形成に必須であることを示した(図)。
Watanabe M., Ito T. and Fukuda A. Effects of taurine depletion on body weight and mouse behavior during development. Metabolites, 2022, 12(7), 631.
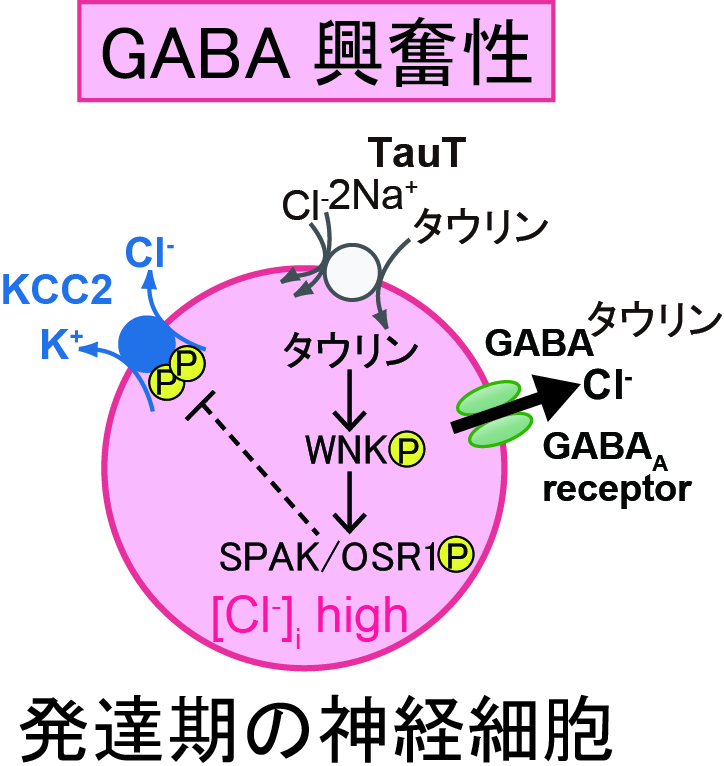
タウリンは中枢神経系に豊富に存在し、神経細胞外ではGABAA受容体のアゴニストとして作用している。細胞内にはタウリントランスポーター(TauT)で取り込まれ、WNK-SPAK/OSR1のリン酸化カスケードを活性化させ、カリウム-クロライド共輸送体(KCC2)の機能を抑制し、胎仔特有のCl-ホメオスタシスを維持することを報告している(図)。本研究では細胞内タウリンの役割についてさらに検討するために、TauT欠損により細胞内タウリンが枯渇しているTauTノックアウトマウスを用いて解析を行ったところ、行動解析では不安様行動、大きな音に対する驚愕反応の低下、また、筋持久力の低下がみられた。生後1週間後から体重の減少が認められ、脳内のSTAT3のリン酸化が亢進していたことから、食欲抑制作用のあるレプチンシグナルが亢進している可能性が示唆された。よって、タウリンは神経機能、筋持久力、エネルギー代謝の維持に重要な役割を持つことが明らかになった。
Watanabe M., Zhang J., Mansuri M.S., Duan J., Karimy J.K., Delpire E., Alper S.L., Lifton R.P., Fukuda A. and Kahle K.T. Developmentally regulated KCC2 phosphorylation is essential for dynamic GABA-mediated inhibition and survival. Science Signaling, 2019, 12, eaaw9315.
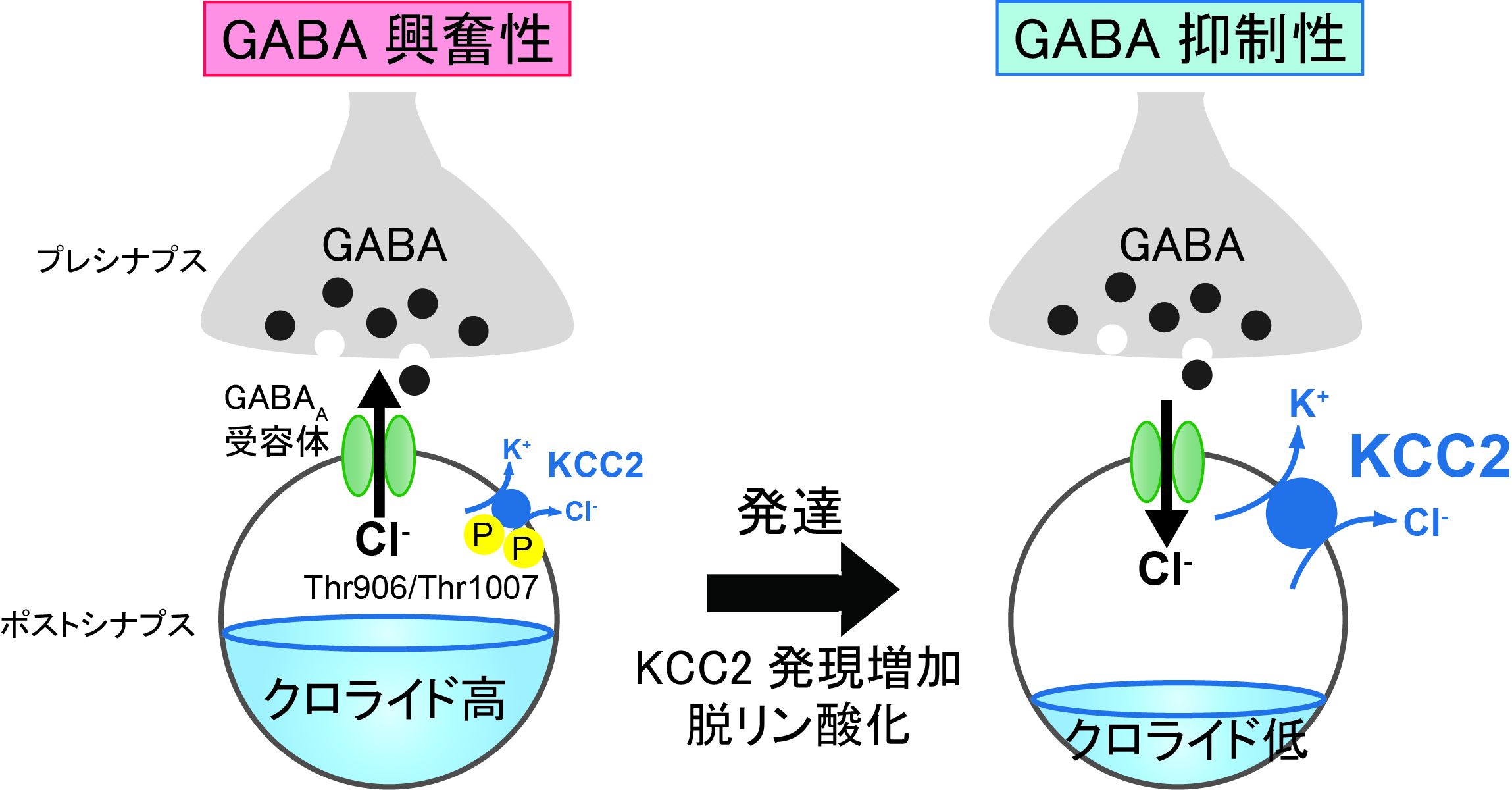
脳内の主要な抑制性伝達物質であるγ-アミノ酪酸(GABA)は発達期には興奮性伝達物質として働き、細胞増殖や移動、神経回路形成に関わるが、発達に伴いカリウム-クロライド共輸送体(KCC2)の機能が高まることにより、GABA作用は興奮性から抑制性に変化する。本研究では、この変化にはKCC2のリン酸化による機能制御が関わっており、発達期にはKCC2の906番目(Thr906)と1007番目(Thr1007)のスレオニン残基がリン酸化されているため機能が抑制されており、発達に伴い脱リン酸化されることでKCC2が機能し始め、GABA作用が興奮性から抑制性になることが明らかになった(図)。発達期にKCC2のThr906とThr1007のリン酸化が適切に制御されることが、抑制性GABA伝達の形成に必須であり、神経発達および生存に重要であることが示された。本論文は掲載号の表紙を飾り、Editorial Boardにより注目論文に選定され、「FOCUS」に紹介された。
Shinmyo Y., Terashita Y., Dinh Duong T. A., Horiike T., Kawasumi M., Hosomichi K., Tajima A. and Kawasaki H. Folding of the cerebral cortex requires Cdk5 in upper-layer neurons in gyrencephalic mammals. Cell Reports, 2017, 20(9), 2131-2143.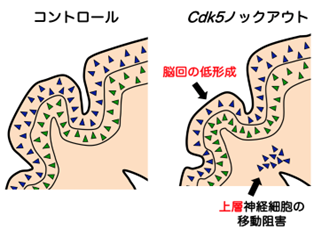
ヒトなどの高等哺乳動物では大脳皮質は特に発達しており、その表面には明瞭なシワ(脳回脳溝)が形成される。進化における脳回脳溝の獲得は高次脳機能の発達の基盤であることから、その形成メカニズムの解明は神経科学の重要研究課題である。本論文では、脳回脳溝などの発達した脳神経構築を持つイタチ科に属するフェレットを用いて脳回脳溝形成機構の一端を明らかにした。独自に開発した遺伝子ノックアウト技術を用いてヒト滑脳症の原因遺伝子であるCdk5遺伝子をノックアウトすると、脳回脳溝の形成が阻害された(図)。さらに解析を進めた結果、大脳皮質下層の神経細胞よりも上層の神経細胞の移動が脳回脳溝形成により重要であることが明らかとなった。つまり、上層の神経細胞の移動による脳表面の拡張が脳回脳溝形成に重要なプロセスであると考えられた。
*Shinmyo Y. (Corresponding author), Riyadh M. A., Ahmed G., Naser I. B., Hossain M., Takebayashi H., Kawasaki H., Ohta K. and Tanaka H. Draxin from neocortical neurons controls the guidance of thalamocortical projections into the neocortex. Nature Communications, 2015, 6, 10232.
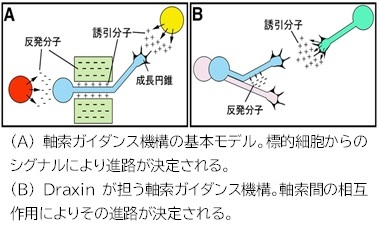
1990年代にNetrinを代表とする神経軸索ガイダンス分子が発見されて以降、神経軸索が標的細胞に導かれるという軸索誘導の基本概念が明らかにされてきた(図A)。しかし、この概念だけでは大脳皮質に見られる複雑な神経回路の形成機構を説明することはできない。本論文では、皮質視床軸索から分泌されるDraxinが視床皮質軸索投射に必須であることを明らかにした。即ち、大脳皮質の神経回路に、神経細胞の「軸索-軸索間の相互作用」が重要であることを示した(図B)。
#Islam S. M., #Shinmyo Y. (co-first author), Okafuji T., Su Y., Naser I. B., Ahmed G., Zhang S., Chen S., Ohta K., Kiyonari H., Abe T., Tanaka S., Nishinakamura R., Terashima T., Kitamura T. and Tanaka H. Draxin, a repulsive guidance protein for spinal cord and forebrain commissures. Science, 323, 388-393, 2009.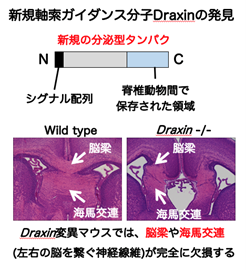
正常な脳神経回路の形成には、発生期に神経軸索ガイダンス分子が担う神経細胞の選択的な軸索形成が必須である。神経回路形成に関わる新規の軸索ガイダンス分子が存在すると考え、分子探索とその機能解析を行った。その結果、脳や脊髄の背側に発現する反発分子を発見し、Draxin(Dorsal repulsive axon guidance protein)と命名した。さらに、Draxin ノックアウトマウスを作成し、その表現型解析を行なった結果、Draxin が大脳のすべての交連神経(脳梁、前交連、海馬交連)の形成に必須であることが明らかとなった。重要な神経軸索ガイダンス分子は長らく発見されていなかったこともあり、この論文はNature Reviews NeuroscienceのResearch Highlightなどで紹介され、さらに、Faculty of 1000 Biologyにおいて'Exceptional'の評価を受けた。
Shinmyo Y., Mito T., Uda T., Nakamura T., Miyawaki K., Ohuchi H. and Noji S. brachyenteron is necessary for morphogenesis of the posterior gut but not for anteroposterior axial elongation from the posterior growth zone in the intermediate-germband cricket Gryllus bimaculatus. Development, 133, 4539-4547, 2006.
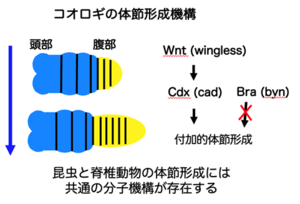 ショウジョウバエはその発生機構が最も理解されている動物である。一方で、ショウジョウバエは昆虫の中でも特殊化した発生様式を持つ。例えば、ショウジョウバエの全ての体節は、多核性胞胚期(多数の核が細胞質を共有している時期)に同時に形成される。他方、コオロギを含む多くの昆虫の体節は、脊椎動物と同様に付加的に形成される。そこで、コオロギにおいて独自に開発した遺伝子機能解析法を用いて初期発生遺伝子群の機能解析を行った。その結果、昆虫と脊椎動物の体節形成には共通の分子メカニズム(Wnt/Cdx経路)が存在することが示唆された。一方、脊椎動物の付加的体節形成に重要なBra (Byn)は、コオロギでは必要ではないことを明らかにした。この成果は、動物の発生システムの進化を理解する上で重要な知見となった。
ショウジョウバエはその発生機構が最も理解されている動物である。一方で、ショウジョウバエは昆虫の中でも特殊化した発生様式を持つ。例えば、ショウジョウバエの全ての体節は、多核性胞胚期(多数の核が細胞質を共有している時期)に同時に形成される。他方、コオロギを含む多くの昆虫の体節は、脊椎動物と同様に付加的に形成される。そこで、コオロギにおいて独自に開発した遺伝子機能解析法を用いて初期発生遺伝子群の機能解析を行った。その結果、昆虫と脊椎動物の体節形成には共通の分子メカニズム(Wnt/Cdx経路)が存在することが示唆された。一方、脊椎動物の付加的体節形成に重要なBra (Byn)は、コオロギでは必要ではないことを明らかにした。この成果は、動物の発生システムの進化を理解する上で重要な知見となった。

